原理
蛋白質は、末端にNH基やCOOH基という解離基をもち、さらに構成アミノ酸の一部にも電荷をもった解離基があるため、泳動緩衝液のpHにより各々の等電点によってプラスやマイナスに帯電する。
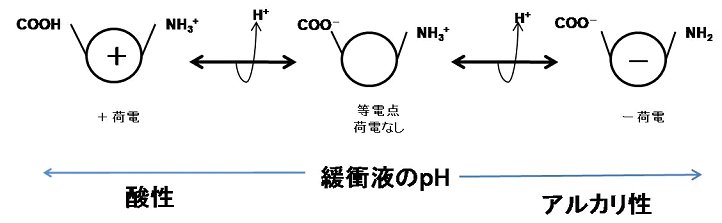
この状態で緩衝液中に電場を生じさせると、プラスに荷電した蛋白は陰極に、マイナスに荷電した蛋白は陽極に向かって移動(電気泳動現象)する。個々の蛋白質は分子量や電荷の違いにより移動度に差が生じ、分画に分けることができる。
蛋白質は、末端にNH基やCOOH基という解離基をもち、さらに構成アミノ酸の一部にも電荷をもった解離基があるため、泳動緩衝液のpHにより各々の等電点によってプラスやマイナスに帯電する。

この状態で緩衝液中に電場を生じさせると、プラスに荷電した蛋白は陰極に、マイナスに荷電した蛋白は陽極に向かって移動(電気泳動現象)する。個々の蛋白質は分子量や電荷の違いにより移動度に差が生じ、分画に分けることができる。